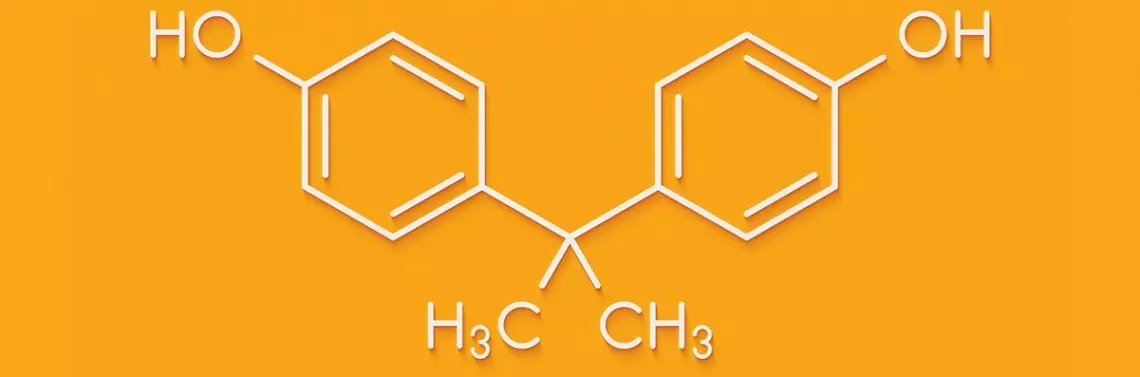
Bisfenol A znalazł zastosowanie zarówno w wielu produktach konsumenckich, w tym w tworzywach sztucznych, takich jak poliwęglany (PC), polichlorek winylu (PVC), żywice epoksydowe, jak i w opakowaniach do żywności (pojemniki, wnętrze konserw), sprzęcie medycznym, kosmetykach, uszczelniaczach dentystycznych, rurach wodociągowych, elektronice, zabawkach dla dzieci, płynach hamulcowych czy nawet paragonach termicznych. Wyroby, które wyprodukowano z zastosowaniem BPA, są przejrzyste, lekkie, wygodne w użyciu oraz odporne na uszkodzenia w transporcie.
Mimo licznych zalet i rocznej produkcji przekraczającej kilka milionów ton, BPA wykazuje potwierdzony wynikami badań szkodliwy wpływ na środowisko naturalne. Związek ten należy do grupy ksenoestrogenów, ponieważ ma zdolność do oddziaływania z układem hormonalnym już przy bardzo niskim zakresie stężeń. Tym samym wyjątkowo kontrowersyjne stało się zastosowanie BPA m.in. do produkcji butelek dla niemowląt (wytworzonych z poliwęglanu). W 2010 r. rząd Kanady zakazał importu i sprzedaży takich wyrobów, a w 2011 r. tożsamą decyzję podjęła Unia Europejska. Działania te stały się podstawą do wzmożonych badań nad toksycznością BPA oraz kolejnych decyzji ograniczających emisję monomeru do środowiska naturalnego.
POLECAMY
Przegląd przez główne analogi BPA
Społeczne zainteresowanie związkami endokrynnie aktywnymi oraz rządowe regulacje dotyczące BPA przyczyniły się do rozwoju i produkcji alternatywnych substancji, które miały zastąpić go w niezliczonych zastosowaniach. Obecnie szereg chemikaliów, które wykazują strukturalne podobieństwo do BPA, wykorzystuje się do produkcji tworzyw sztucznych (Chen i wsp. 2016). Substancje te mają wspólną strukturę dwóch hydroksyfenylowych grup funkcyjnych i łącznie określane są jako analogi bisfenolu. Dotychczas udokumentowano wykorzystanie 16 takich substancji do zastosowań przemysłowych. Jednakże – jak wskazują najnowsze wyniki badań – substancje te wykazują toksyczność zbliżoną lub znacznie przewyższającą związek macierzysty.
Bisfenol F (BPF), bisfenol S (BPS), bisfenol AF (BPAF) oraz etery diglicydylowe bisfenolu A i F (BADGE, BFDGE) należą obecnie do głównych substytutów BPA w produkcji poliwęglanowych tworzyw sztucznych i żywic epoksydowych. Czy jesteśmy narażeni na kontakt z wymienionymi substancjami? Bisfenol F ma szeroki zakres zastosowań i wykorzystywany jest przy produkcji lakierów, podkładów, klejów do tworzyw sztucznych, a także w uszczelniaczach dentystycznych, protezach jamy ustnej, substytutach tkanek czy powłokach do pakowania żywności (Danzl i wsp. 2009). Ponadto BPF jest jednym z najczęściej identyfikowanych analogów BPA w produktach spożywczych, takich jak żywność w konserwach, produkty mleczne, oleje, ryby i owoce morza, mięso, owoce i warzywa. Jak wy...
Pozostałe 90% treści dostępne jest tylko dla Prenumeratorów
- 6 wydań czasopisma "Naturoterapia w praktyce" w roku + wydania specjalne
- Nielimitowany dostęp do całego archiwum czasopisma
- Dodatkowe artykuły i filmy
- ...i wiele więcej!